エノールシリルエーテルはリチウムエノラートの次に有用な反応剤です。ケイ素はリチウムほど電気的に陽性ではないため、リチウムエノラートより安定で、反応性が低いです。エノールシリルエーテルは、エノラートをケイ素の求電子剤で処理することにより調製できます。ケイ素求電子剤は「ケイ素が硬い」、「$\rm Si-O$結合が非常に強い」ため、必ずエノラートの酸素と反応します。最も一般的なケイ素求電子剤はトリクロロメチルシラン$\rm Me_3SiCl$で、工業的に大量に合成されています。
ケイ素ー酸素結合は非常に強い結合であるため、ケイ素は強塩基が共存しなくてもカルボニル化合物の酸素と反応してエノールシリルエーテルを生成します。
この反応機構は下の2つが考えられますが、どちらが正しいのかはよくわかっていません。
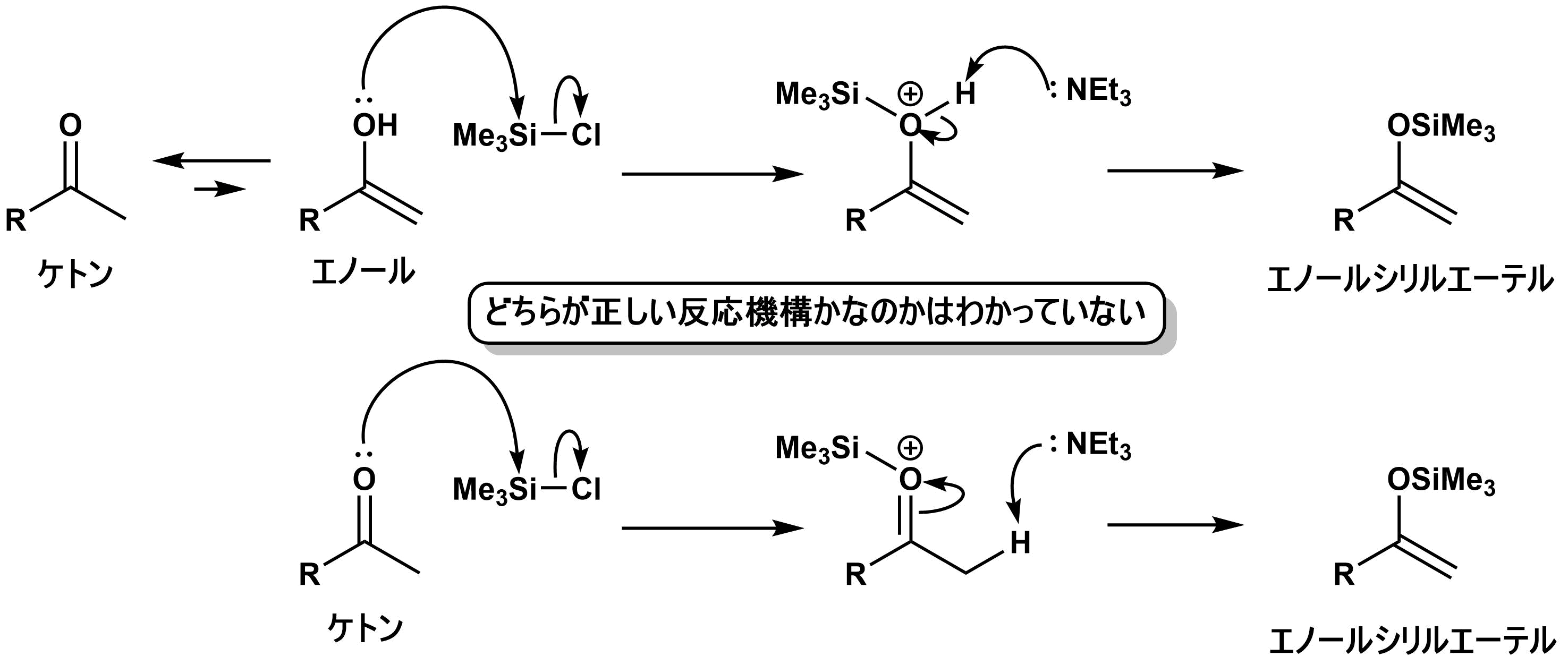
このエノールシリルエーテルは$\rm TiCl_4$や$\rm SnCl_4$などのLewis酸存在下で$\rm S_N1$反応性の高いカルボカチオンと反応しアルキル化できます。
まず、$\rm S_N1$反応性の高いカルボカチオンを作るために、ハロゲン化アルキルからLewis酸を用いて脱離基(ハロゲン)を脱離させます。その後、そのカルボカチオンがエノールシリルエーテルと反応してアルキル化が起きます。