$\rm S_N1$反応と$\rm E1$反応に共通なイオン化は、中間体カチオンの生成のしやすさ、すなわち、$\rm R^+$の安定生によって支配されます。しかし、分子内に求核性を持つ置換基があるとき、その関与によって、反応が促進される場合があります。
隣接基関与ではない通常のE1や$\rm S_N1$反応の例としては、以下のようなものがあります。以下の例では、$\rm MeS$基が共役効果によって、$α$位のカルボカチオンを大きく安定化するため、反応を促進しています。
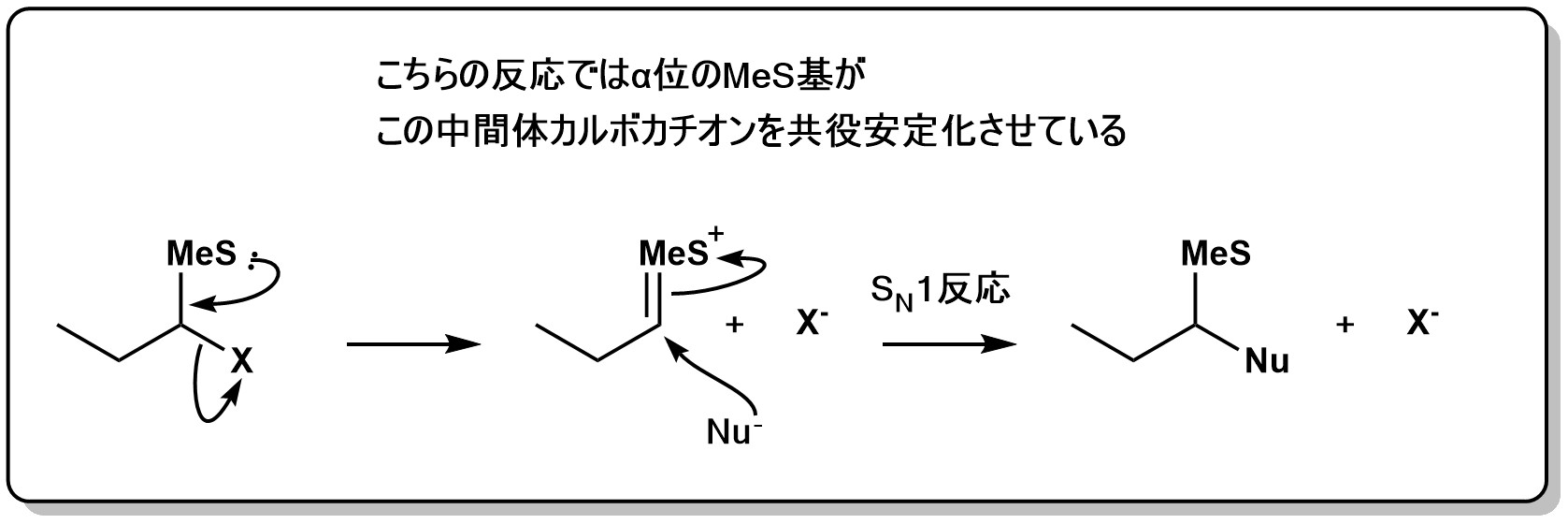
しかし、以下のように、$β$位に$\rm MeS$基がついている場合は共役安定化には全く関係がありません。それにもかかわらず$α-{\rm MeS}$基と同じような反応促進効果を示します。このような直接共役ではなく、このような結合を隔てた分子内置換基による反応の促進を隣接基質関与といいます。この隣接基関与がおこると、異常に反応速度が増大したり、立体化学の保持や転移が起こったりします。隣接基関与では、分子内$\rm S_N2$機構によって立体化学の保持が起こっています。

転移が起こる隣接基関与の例も見てみましょう。
次のクロロメチル基をもつ五員環アミンは六員環アミンに転移します。
この反応機構は以下のような分子内$S_N2$機構です。
参考)奥山 格 「電子の動きで見る有機反応の仕組み」東京化学同人 pp.42~45