(a)
塩基性条件下では以下のような反応がおきます。臭素は電子求引性なので、一度臭素とα水素が置換すると、残りのα水素の酸性度が高くなります。そのため、より$\rm OH^-$に求核攻撃されて脱離しやすくなります。そのため、α水素はすべて臭素と置換されます。すべてのα水素が置換された、$\rm -CBr_3$はカルボアニオンが$\rm Br$で安定化するため、脱離能があります。そのため、アシル置換反応が起こり、最終的に安息香酸とトリブロモメタン(ブロモホルム)$\rm HCBr_3$が生成します。このように、ハロホルム$\rm HCX_3$が生成するため、ハロホルム反応と呼ばれています。
酸性条件下では塩基性条件とは異なり、α水素は一度しか臭素と置換しません。なぜなら、一度臭素とα水素が置換すると、カルボニル酸素の塩基性が減少するからです。(臭素は電子求引性なので、カルボニル酸素の$δ^-$性を減少させる)そのため、反応は臭素が一度置換して、そこで止まります。
※以上の説明が基本ですが、じつは、酸性条件下で反応が1置換で止まるのは、「ハロゲンを1当量だけしか用いないから」といったほうが正解です。実は、ハロゲンがもっとあれば酸性条件がでもハロゲン化は続けて起こりえます。ただ、やはり、第二のハロゲン化は最初に比べて明らかに遅いのは確かです。その理由は上述の理由(ブロモケトンはケトンよりも塩基性が低下しているので、プロトン化されるケトンの割合が減るため、反応が進行しにくくなる)に加えて、反応中間体の多くが正電荷をを持っており、ハロゲンが置換することによってこれらが不安定化されるという理由もあります。しかし、次の問題である(b)では「簡潔に述べよ」とあるので、ハロホルム反応の酸性の増大、酸性条件での塩基性の減少を対応させて解答してあります。
参考)ウォーレン有機化学 上 第二版 p471、p473
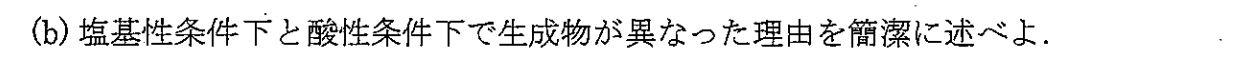
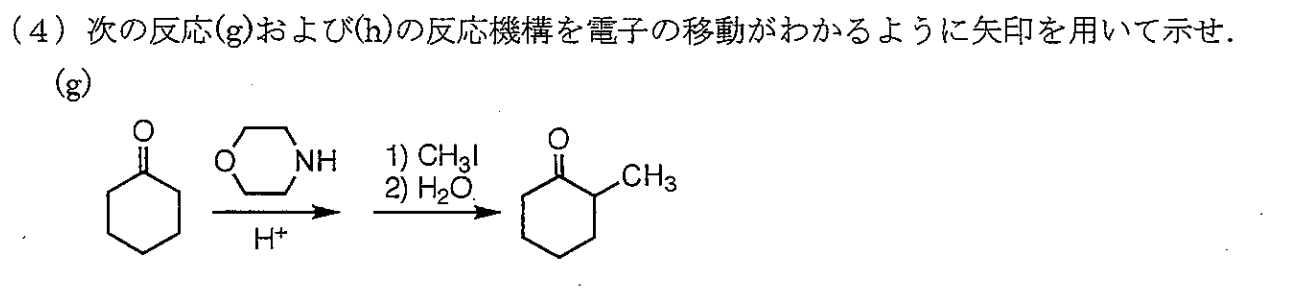
塩基性条件ではα水素が引き抜かれることによって反応が進行する。一度α水素が臭素と置換すると、残りのα水素の酸性度が増大するため、より反応が起こりやすくなる。
一方、酸性条件ではカルボニル酸素がプロトン化されることによる反応が進行する。こちらは一度α水素と置換すると、カルボニル酸素の塩基性が減少するため、反応が起こりにくくなる。そのため、反応がそこでとまり、1置換にとどまる。
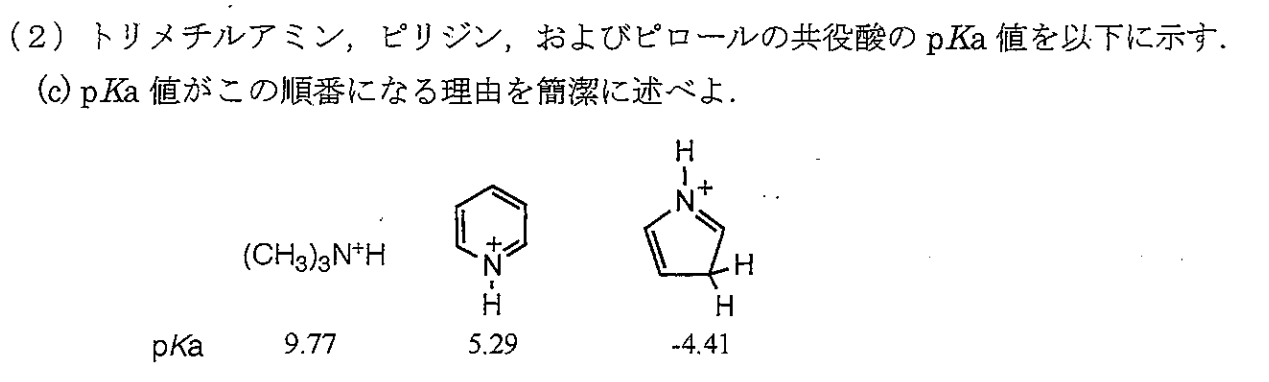 ピリジンの窒素の非共有電子対は$\rm sp^2$軌道に入っているのに対し、トリメチルアミンの窒素の非共有電子対は$\rm sp^3$軌道に入っている。入っている軌道のp性が大きくなるほど、非共有電子対のエネルギーは高く、原子核から離れた位置に存在する確率が高いため、塩基性が強い。つまり、トリメチルアミンのよりもp性の小さいピリジンのほうが塩基性が低い。また、ピロールの非共有電子対は芳香族系に取り込まれいるため、ピロールのほうがピリジンよりさらに塩基性が低い。よって、塩基性の強さの順番がトリメチルアミン>ピリジン>ピロールとなるため、塩基性が高いほどその共役酸が安定ということなので、pKaもその順番になる。
ピリジンの窒素の非共有電子対は$\rm sp^2$軌道に入っているのに対し、トリメチルアミンの窒素の非共有電子対は$\rm sp^3$軌道に入っている。入っている軌道のp性が大きくなるほど、非共有電子対のエネルギーは高く、原子核から離れた位置に存在する確率が高いため、塩基性が強い。つまり、トリメチルアミンのよりもp性の小さいピリジンのほうが塩基性が低い。また、ピロールの非共有電子対は芳香族系に取り込まれいるため、ピロールのほうがピリジンよりさらに塩基性が低い。よって、塩基性の強さの順番がトリメチルアミン>ピリジン>ピロールとなるため、塩基性が高いほどその共役酸が安定ということなので、pKaもその順番になる。
参考)ウォーレン有機化学 上 第二版 p175