
$$\rm 2 KClO_3 → 2 KCl + 3 O_2$$
 $$\rm CaC_2+2H_2O→Ca(OH)_2+HC≡CH$$
$$\rm CaC_2+2H_2O→Ca(OH)_2+HC≡CH$$
 アジ化ナトリウムの分解反応
アジ化ナトリウムの分解反応
$$\rm 2NaN_3→2Na+3N_2$$
Naを安定化させる反応
$$\rm 10Na+2KNO_3→K_2O+5Na_2O+N_2\\
\rm K_2O+Na_2O+SiO_2→ガラス$$
(g)
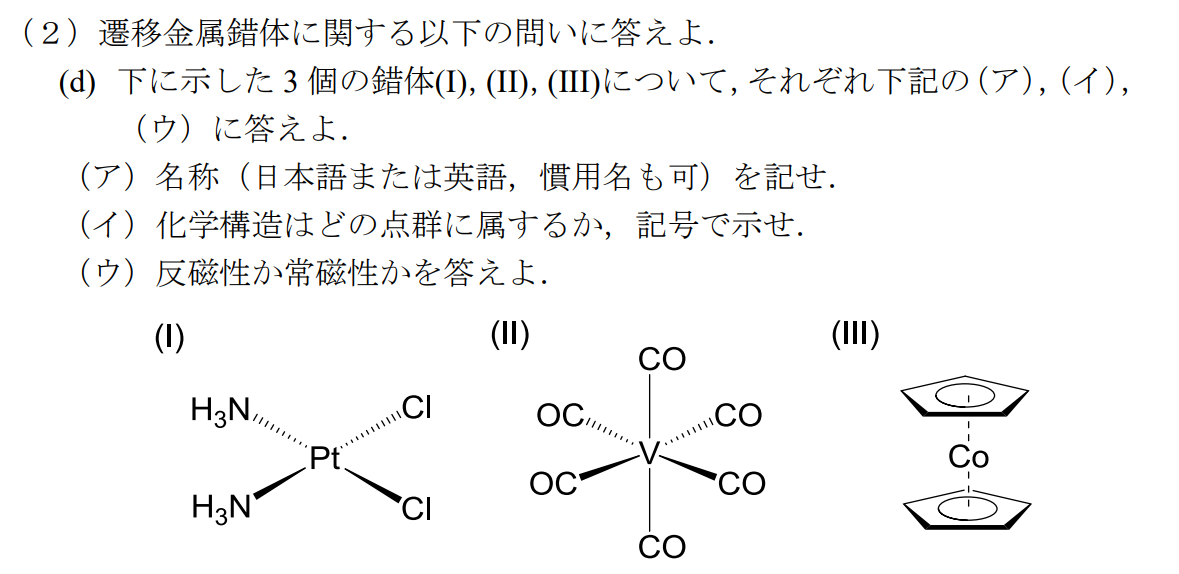 (ア)
(ア)
錯体の命名は、中心金属原子の酸化数からはじめ、配位指名をアルファベット順で並べます。
(Ⅰ)
ジアンミンジクロリド白金(Ⅱ)
シスプラチン(慣用名)
※
錯体は2つのアニオン性配位子($\rm Cl^{-}$)、2つの中性配位子($\rm NH_3$)をもち、配位子全体の電荷がー2です。よって、錯体全体で中性なので、白金は+2つまり、酸化数はⅡとなります。よって、錯体名は、
ジアンミンジクロリド白金(Ⅱ)になります。
(Ⅱ)ヘキサカルボニルバナジウム
(Ⅲ)コバルトセン(慣用名)
(イ)
(Ⅰ)$C_{\rm 2v}$(※参考 $\rm trans-[PtCl_2(NH_3)_2]$の点群は$ D_{2h}$です。)
(Ⅱ)$O_{\rm h}$
(Ⅲ)$ D_{\rm 5d}(重なり形) \ or \ D_{\rm 5h}(36°ねじれ型)$
(ウ)
(Ⅰ)Ptは$\rm d^{8}$で、かつ平面正方形なので、反磁性となる。
(Ⅱ)Vは$\rm d^{3}$で、八面体構造なので、常磁性になる。
(Ⅲ)19電子錯体なので、常磁性になる。
※参考)さまざまな構造での結晶場分裂の図
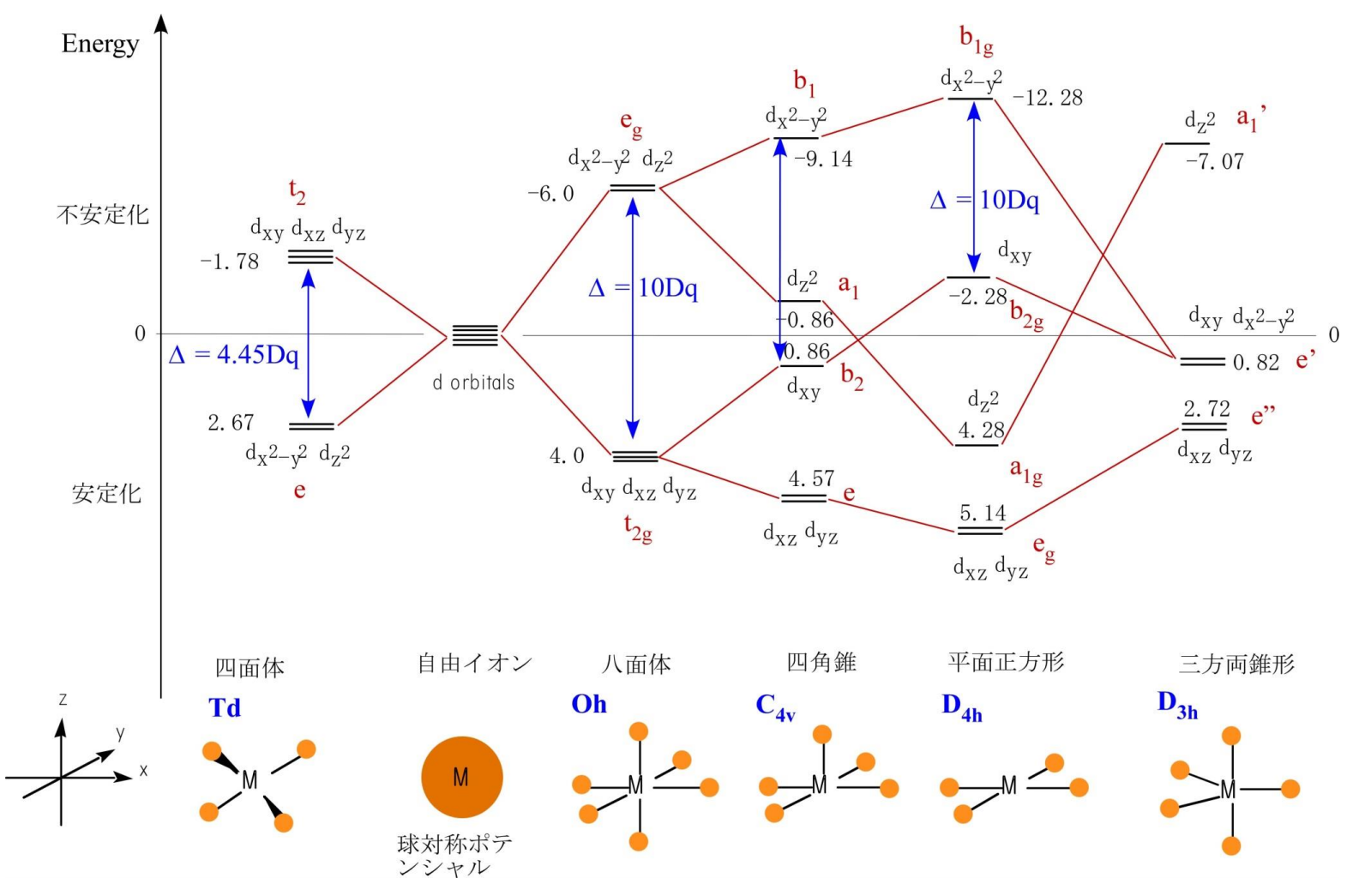 ※引用
※引用
http://www.chem.nara-wu.ac.jp/~tanase/ClassesInfo/Coordination%20Chemistry%20part2.pdf

![]()
 [解答]
[解答]
(1)式は、2×(3)-(2)で作ることができる。よって、
反応(1)のギブズエネルギーは-0.796×4-(-0.850×2)=1.808[eV]
よって、反応(1)はニ電子反応であるから、答えは、
1.808÷2=0.904[V]
参考ページ)Latimer図
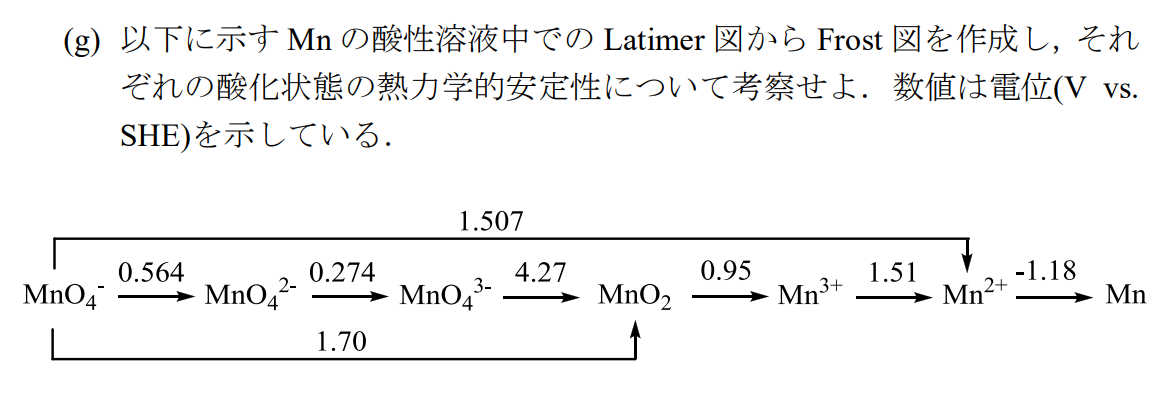
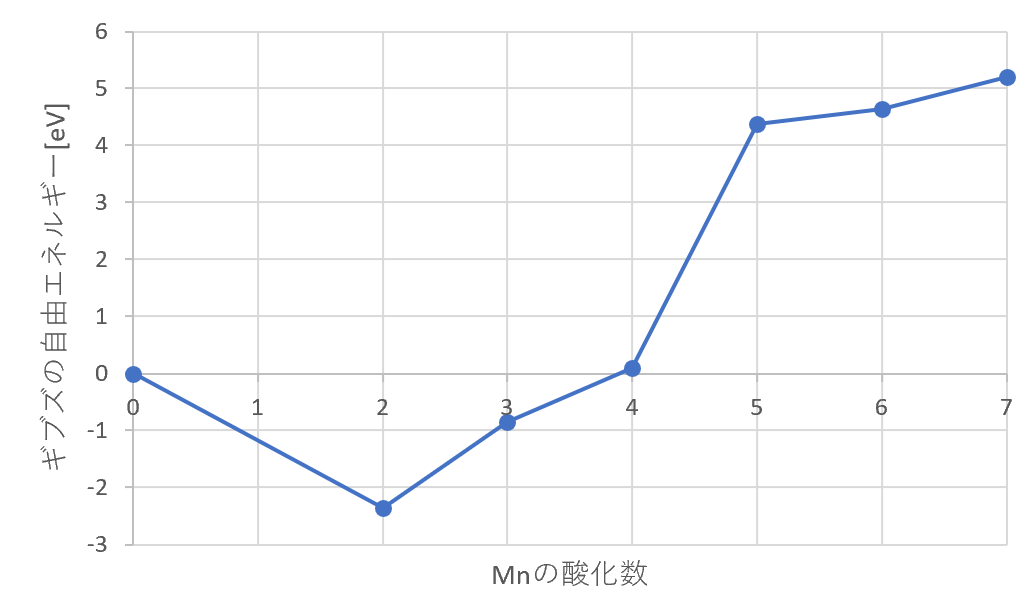 以上のFrost図より、酸性溶液中では$\rm Mn^{2+}$が最も安定に存在することがわかる。また、$\rm Mn^{3+}$は$\rm Mn^{2+}とMnO_2$に、$\rm MnO_4^{3-}$は$\rm MnO_2とMnO_4^{2-}$に不均一化することもわかる。
以上のFrost図より、酸性溶液中では$\rm Mn^{2+}$が最も安定に存在することがわかる。また、$\rm Mn^{3+}$は$\rm Mn^{2+}とMnO_2$に、$\rm MnO_4^{3-}$は$\rm MnO_2とMnO_4^{2-}$に不均一化することもわかる。
参考ページ)Latimer図