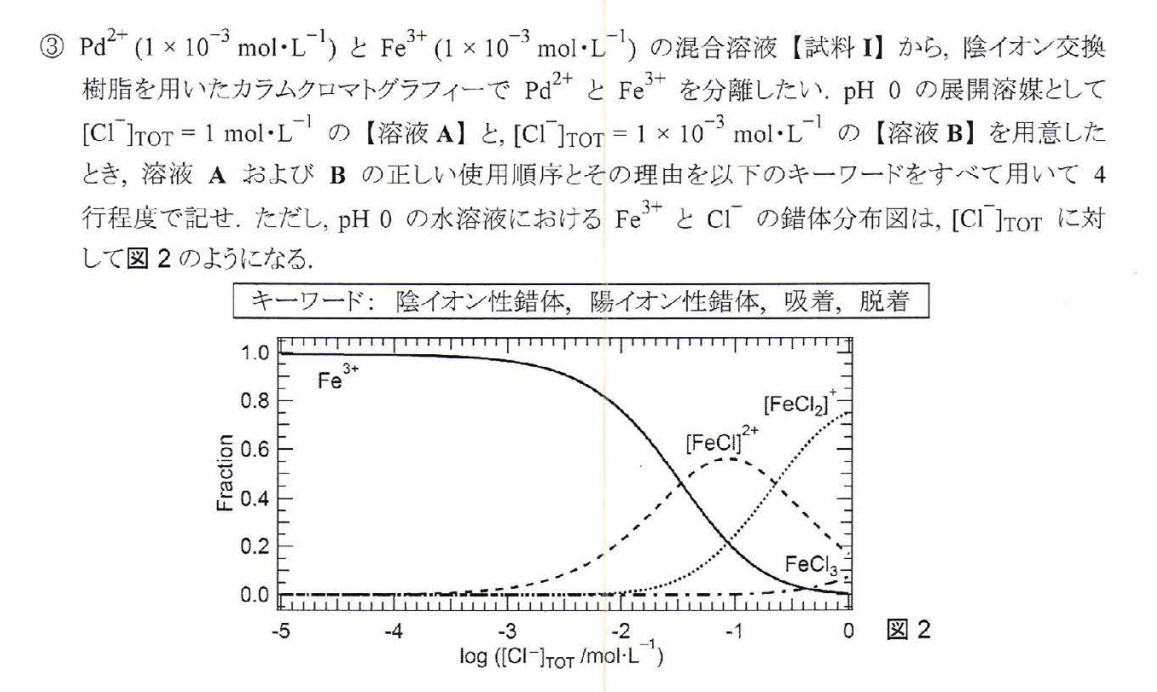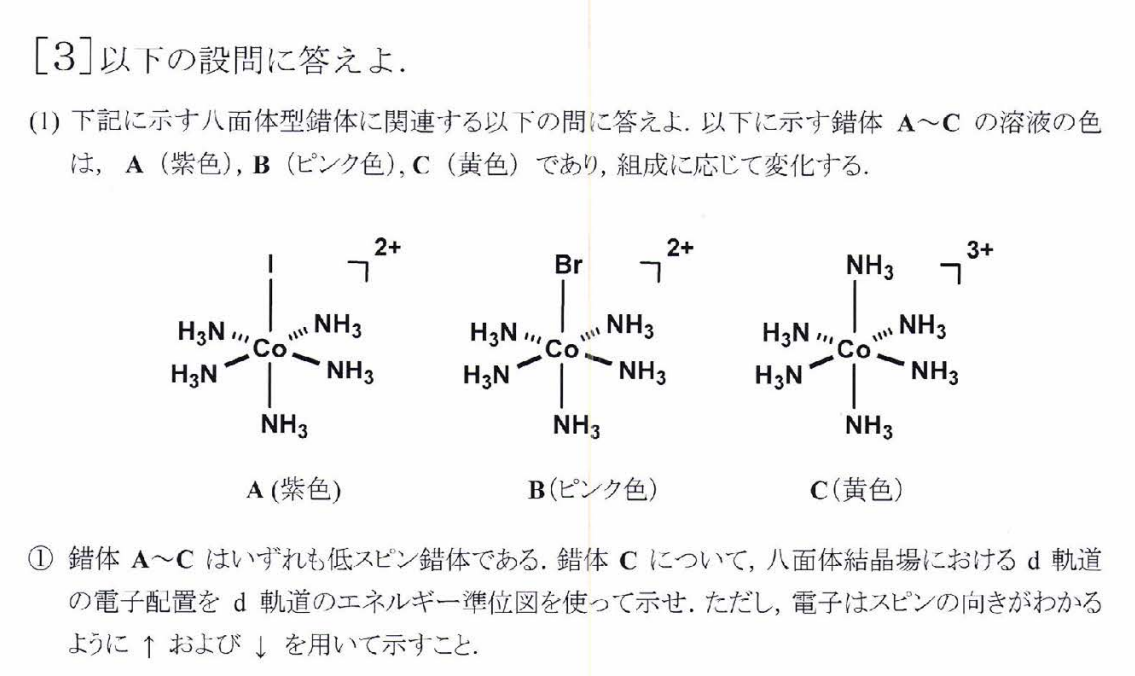
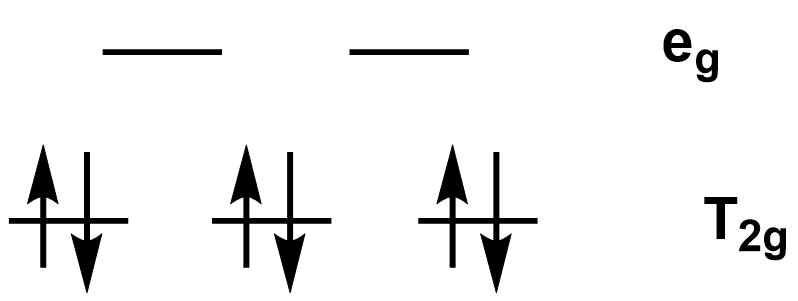
 \begin{eqnarray}
\begin{eqnarray}
(高スピンを取るときの不安定化エネルギー)&>&(低スピンを取るときの不安定化エネルギー) \\
2Δ_o+P&>&3P \\
P&<&Δ_o \\
P&<&\f{22900}{83.6} \\
P&<&273.9[{\rm kJ/mol}] \\
\end{eqnarray}
よって、スピン対生成エネルギーは$\rm 273.9[{kJ/mol}]$となる。

(a)π供与性 (b)$t_{\rm 2g}$ (c)減少 (d)緑色 (e)長波長
※
(a)に関しては、ハロゲンが出てきており、ハロゲンはπ供与性であるということから判断しました。
(σ供与性とπ受容性は増大するほど、どちらも$Δ_o$を増加させるという同じ方向の性質であるということも判断要因の一つであると思います。)
また、π受容性配位子の充填π軌道も、π供与性配位子の空軌道(π*軌道)もどちらも$\rm t_{2g}$ですので、金属の$t_{2g}$軌道と相互作用します。なので、(b)の答えは$t_{2g}$です。
紫色の補色は黄色
ピンクの補色は緑色
黄色の補色は紫色です。
つまり、π供与性が大きくなるほど(π供与性の順序$\rm I^->Br^->NH_3$)$Δ_{\rm o}$が減少して長波長になっていることがわかります。(波長の長さ黄色>緑色>紫色)
参考)ハウスクロフト無機化学 下 第3版 p639~p641
 COのほうがアンミン配位子よりもπ受容性が高い。π受容性の増大は$t_{2g}$準位を安定化させるため、$Δ_{\rm o}$は増大する。
COのほうがアンミン配位子よりもπ受容性が高い。π受容性の増大は$t_{2g}$準位を安定化させるため、$Δ_{\rm o}$は増大する。
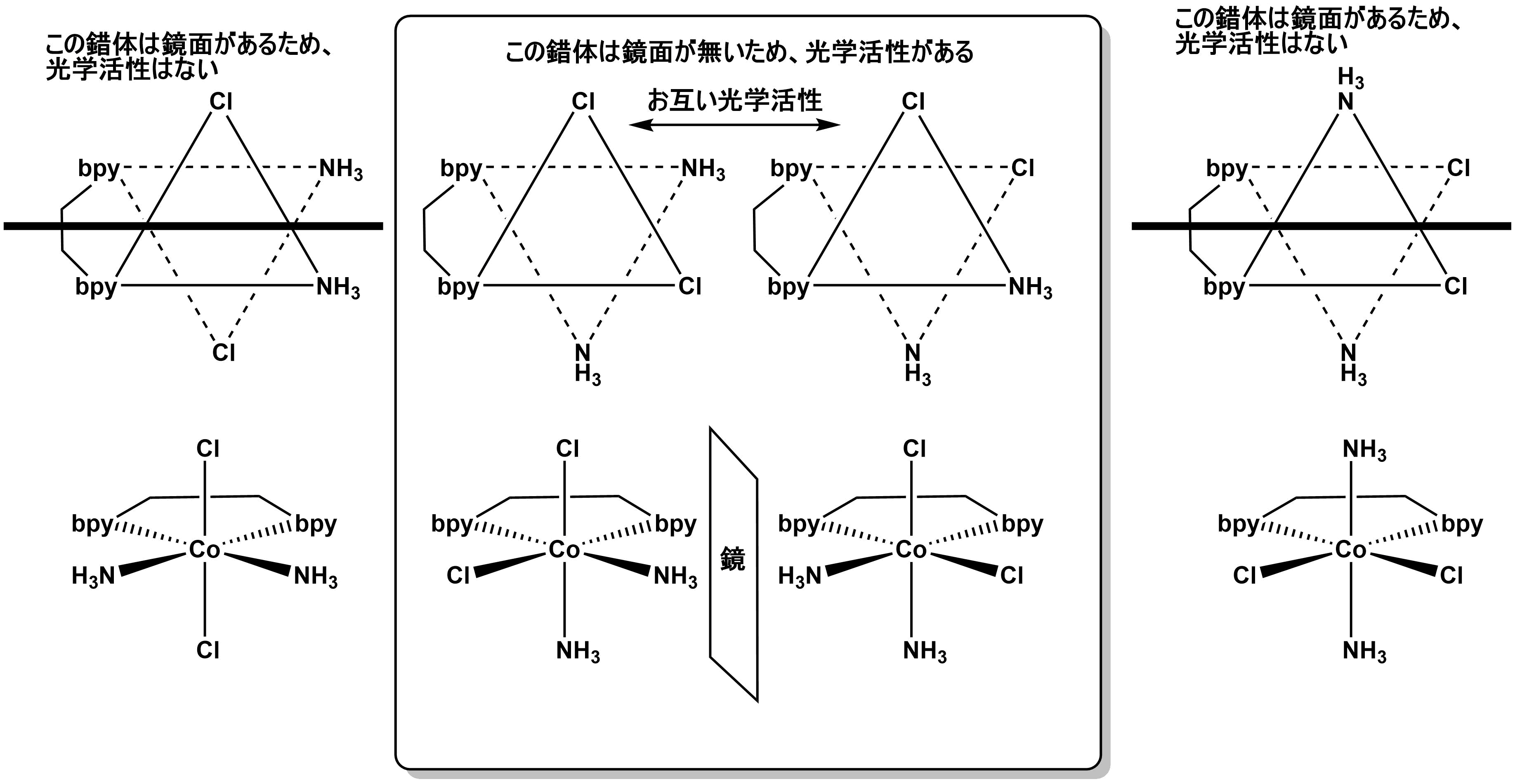
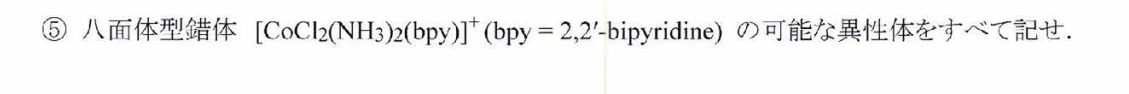 以下の4つです。上は八面体錯体を$C_3$軸から見たときの図。下はそれに対応する構造で、この4つが解答となります。
以下の4つです。上は八面体錯体を$C_3$軸から見たときの図。下はそれに対応する構造で、この4つが解答となります。
 \begin{eqnarray}
\begin{eqnarray}
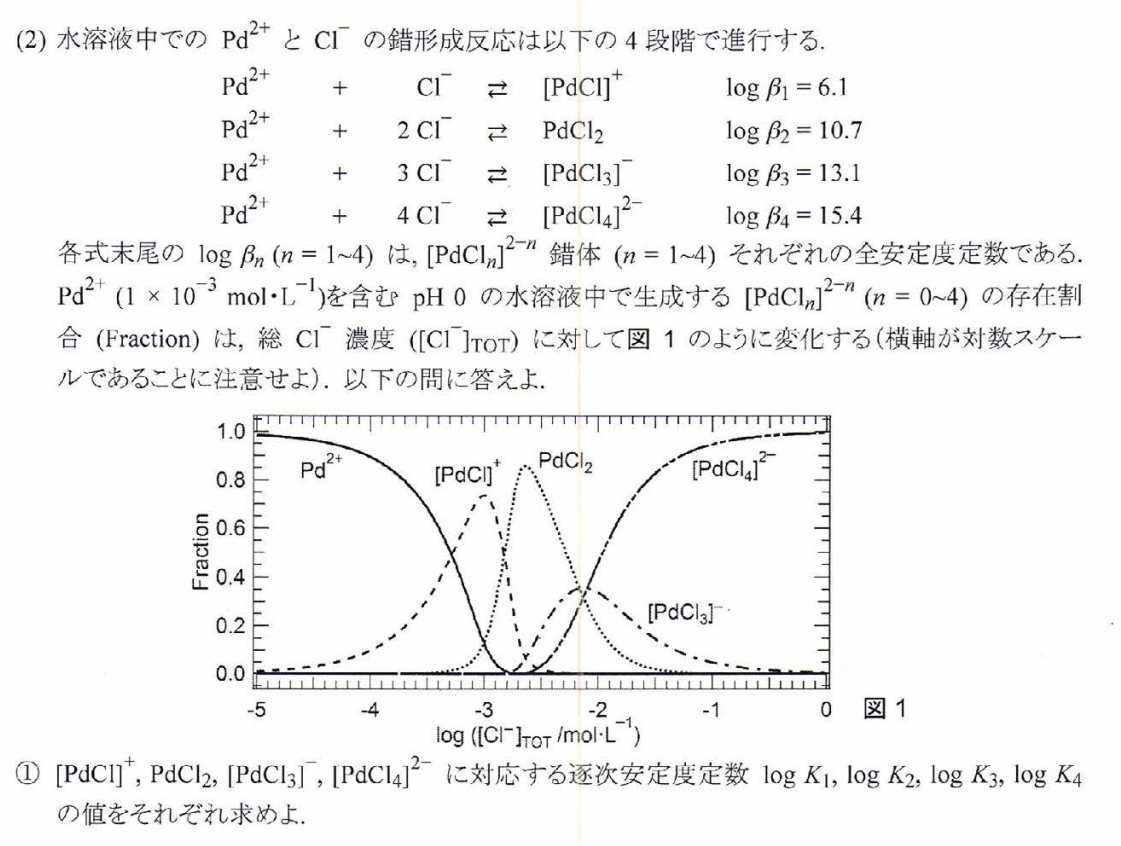
\log K_1&=&6.1 \\
\log K_2&=&10.7-6.1=4.6 \\
\log K_3&=&13.1-10.7=2.4 \\
\log K_4&=&15.4-13.1=2.3 \\
\end{eqnarray}
 Pdは酸化力のある酸に溶けやすい性質を持っている。硝酸に塩酸を混合することで、塩化ニトロシルというより酸化力が強い化合物ができるため、溶けやすくなる。塩酸単体では酸化力がないため、ほとんど溶けない。
Pdは酸化力のある酸に溶けやすい性質を持っている。硝酸に塩酸を混合することで、塩化ニトロシルというより酸化力が強い化合物ができるため、溶けやすくなる。塩酸単体では酸化力がないため、ほとんど溶けない。
※硝酸に塩酸を加えたものはいわゆる王水と呼ばれるものです。
参考)こちらのサイト