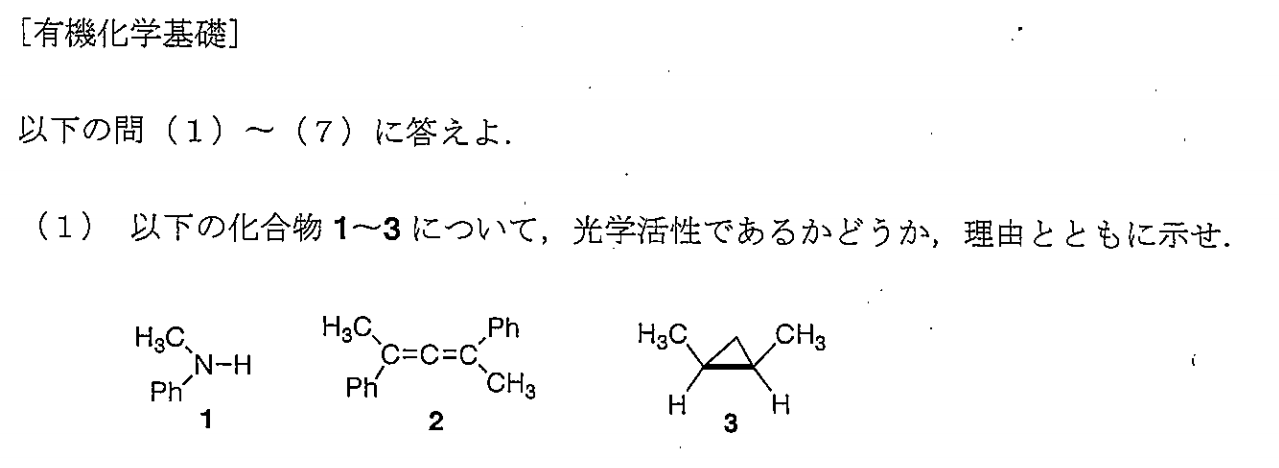
- 光学活性である。
理由:Nは$\rm sp^3$混成軌道をとっており、三角錐型である。そのため、不斉炭素原子と同様に、光学活性をもつ。 - 光学活性である。
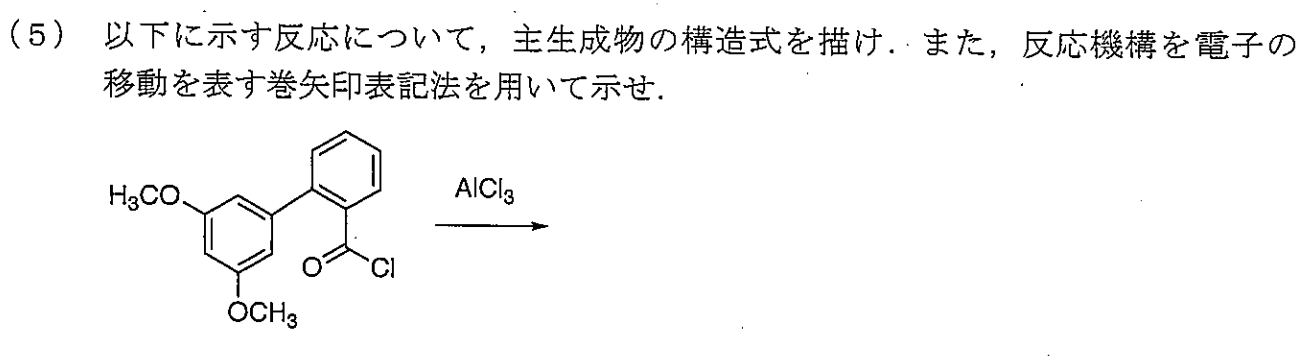
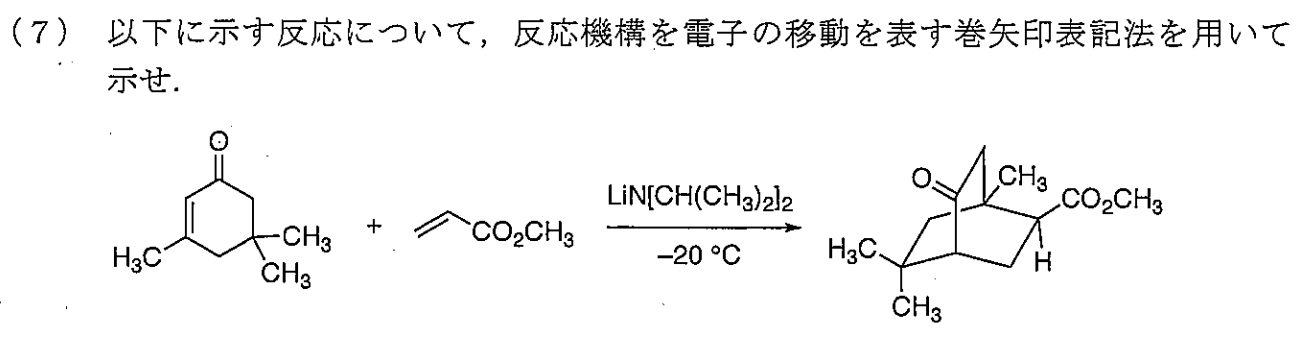
理由:2つの二重結合は、お互い90°ねじれている。そのため、いわゆる軸不斉をもつ - 光学活性ではない。
理由:対称面をもつため。
 4のほうが酸性度が高い。
4のほうが酸性度が高い。
理由:4の共役塩基は6π電子系の芳香族性を獲得して安定であるが、5の共役塩基は8π電子系になり、芳香族性を持たず、安定化しないため。
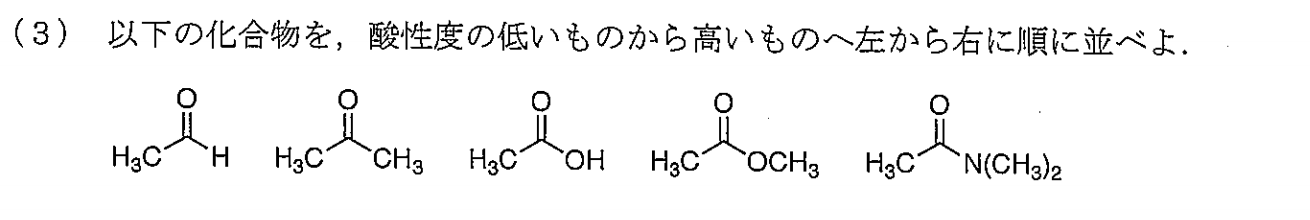 $$\rm CH_3CON(CH_3)_2 \ CH_3COOCH_3 \ CH_3COCH_3 \ CH_3CHO \ CH_3CO_2H$$
$$\rm CH_3CON(CH_3)_2 \ CH_3COOCH_3 \ CH_3COCH_3 \ CH_3CHO \ CH_3CO_2H$$
酸性度の順番は
カルボン酸>アルデヒド>ケトン>エステル>アミドとなります。
カルボニル化合物では全て、共役塩基の負電荷はカルボニル酸素上に分散するので、カルボニル化合物のα水素は酸性が高いです。
カルボン酸は共役塩基が他の共役塩基と比べてとても安定であるため、酸性度が高くなります。
それ以外のカルボン酸はカルボニル酸素についている官能基の電子供与性が高ければ高いほど酸性度は低くなります。(※こちらはネットで見つけた資料です。参考にしてください。)
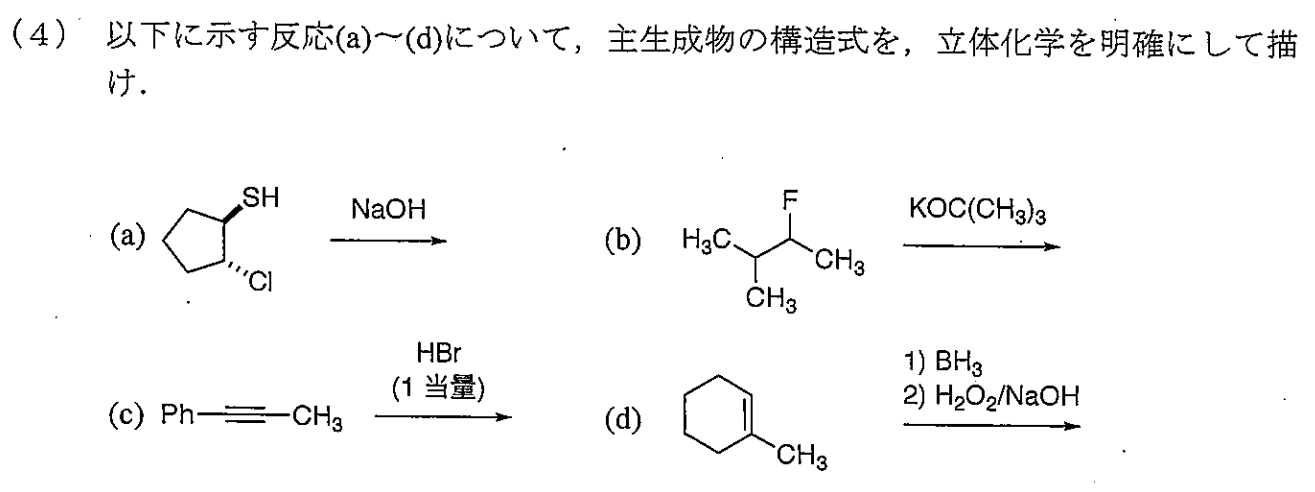
(a)
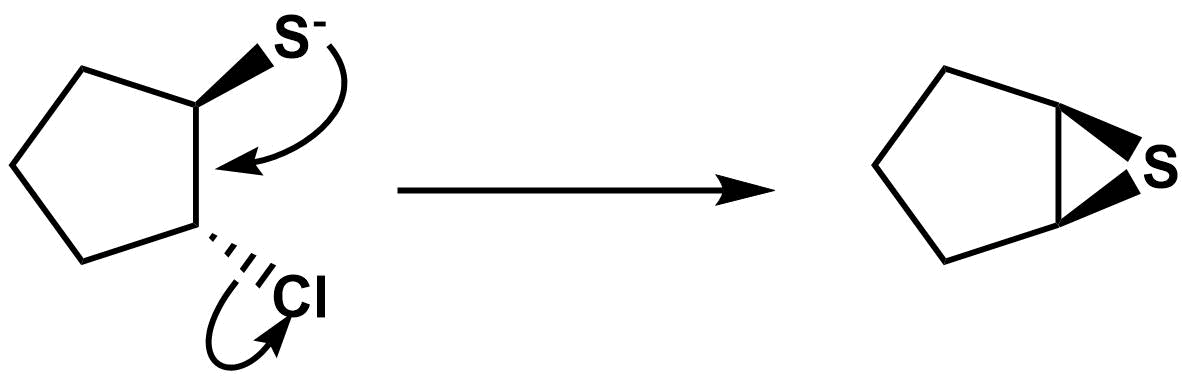
チオール$\rm RSH$はアルコールよりも酸性が高いです。また、大きくて塩基性の低いチオラートイオンは高エネルギーの既占軌道をもち軟らかい求核剤なので、より軟らかい飽和炭素原子を攻撃します。つまり、$\rm S_N2$置換が起こりやすいということです。そのため、分子内$\rm S_N2$反応が起こり、スルフィドが得られると思われます。
参考)ウォーレン有機化学 下 第二版 p685
(b)
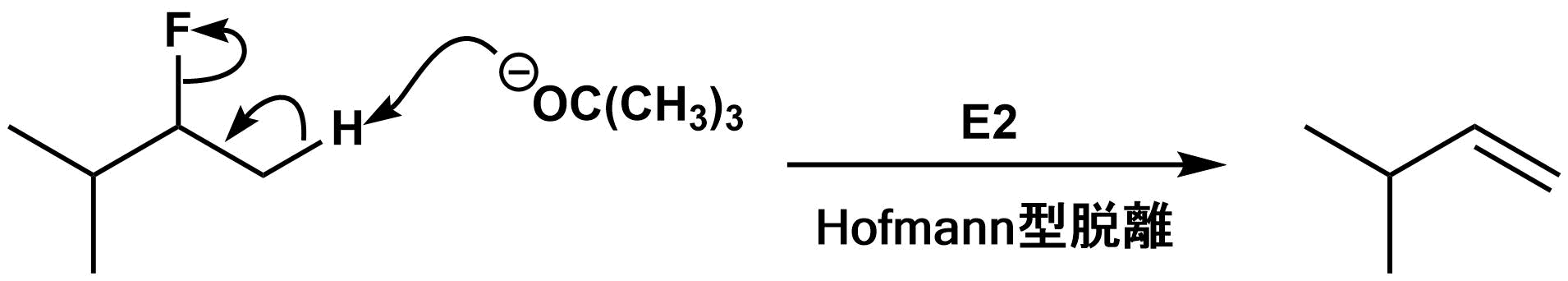
これは脱離の配向性の問題です。2級及び3級化合物からの脱離は複数の生成物を与える可能性があり、脱離の配向性には、Sayzeff型脱離とHofmann型脱離の2種類があります。Saytzeff型脱離は二重結合についた置換基が最も多くなるように、Hofman型脱離は二重結合の周りのち換気が最も少なくなるような方向へ進む脱離反応です。一般にSaytzeff型生成物のほうがHofmann型生成物よりも熱力学的に安定です。一般的に,E1脱離では、Saytzeff型脱離が起こりますが、この反応は、$\rm F$の脱離能の低さから、E1反応ではなく、E2反応であると考えられます。E2反応では、E1反応のように、必ずしも熱力学的に安定な生成物ができるとは限りません。E2反応では、経験的に、
①脱離基の脱離能が低いほどHofmann脱離が起こりやすい。
②ハロゲン化アルキルでは、塩基が嵩高いほどHofmann脱離が起こりやすい。
ということが知られています。よって、この反応では、①も②も満たすので、熱力学的に不安定なHofmann型E2脱離を起こします。
参考)有機化学演習 三共出版 p105
(c)
中間体には二通り考えられますが、上記のように、ベンゼン環には電子供与型共鳴安定化があるため、上記のような経路を通り、生成物ができると思われます。
参考)有機化学演習 三共出版 p86
(d)
ヒドロホウ素化-酸化によるヒドロキシ基の付加は逆マルコフニコフ則で起こります。