
水素分子$\rm H_2$には2つの形が存在し、これらでは2つの核スピンの相対的な向きが異なっている。オルト水素の核スピンは互いに平行($\rm I=1$:三重項)であり、パラ水素の核スピンは互いに反平行($\rm I=0$:一重項)になっている。$T=0$では水素は100%がパラの状態であるが、室温では$オルト水素:パラ水素=3:1$の比率になる。
参考ページ)オルト水素とパラ水素

三中心ニ原子結合の例としてジボランを挙げる。ジボランは以下のような構造をとる。
$\rm B$原子の価電子の数は3であり、$sp^3$混成軌道の3つに不対電子が存在する。そのうち2つは末端の水素原子$\rm H_1$の不対電子と電子対結合して、結合次数1の$\rm B-H_1$結合を作る。残りの$\rm B$原子の不対電子1個と架橋水素原子$\rm H_2$の$1s$電子及び隣の$\rm B$原子の空の$sp^3$混成軌道を使って、架橋部分の$\rm B-H_2-B$結合が作られる。このように、三中心が2電子で結合している結合を三中心二電子結合といい、この結合の結合次数は$\f12$で、$\rm B-H_1$より$\rm B-H_2$の結合距離の方が長い。
参考ページ)三中心二電子結合

四塩化チタンと有機アルミニウム化合物を混合したチーグラー・ナッタ触媒によるオレフィンの重合反応のことを指す。代表的な例にポリエチレンがあるが、この方法で作るポリエチレンは枝分かれが少なく、結晶性が高い。
※
ドイツ人化学者のチーグラーはトリエチルアルミニウムを塩化チタン(Ⅳ)と炭化水素溶媒中で混合すると、褐色の懸濁液になり、それが室温、大気圧下でエチレンを重合して、ポリエチレンを生成することを発見した。この高密度高分子は、これまでの伝統的方法だった高温高圧下で製造される低密度ポリエチレンに比べて多様な用途を生んだ。(チーグラー・ナッタ重合によってできるポリエチレンは分子鎖の枝分かれが少なく、結晶性が高いです。)この触媒は固体の塊を生成するので、触媒系は不均一である。反応は配位不飽和なチタン中心で進行する。正確な機構はまだ解明されていないが、以下のコジー・アルマン機構が可能性の高い機構として広く受け入れられている。
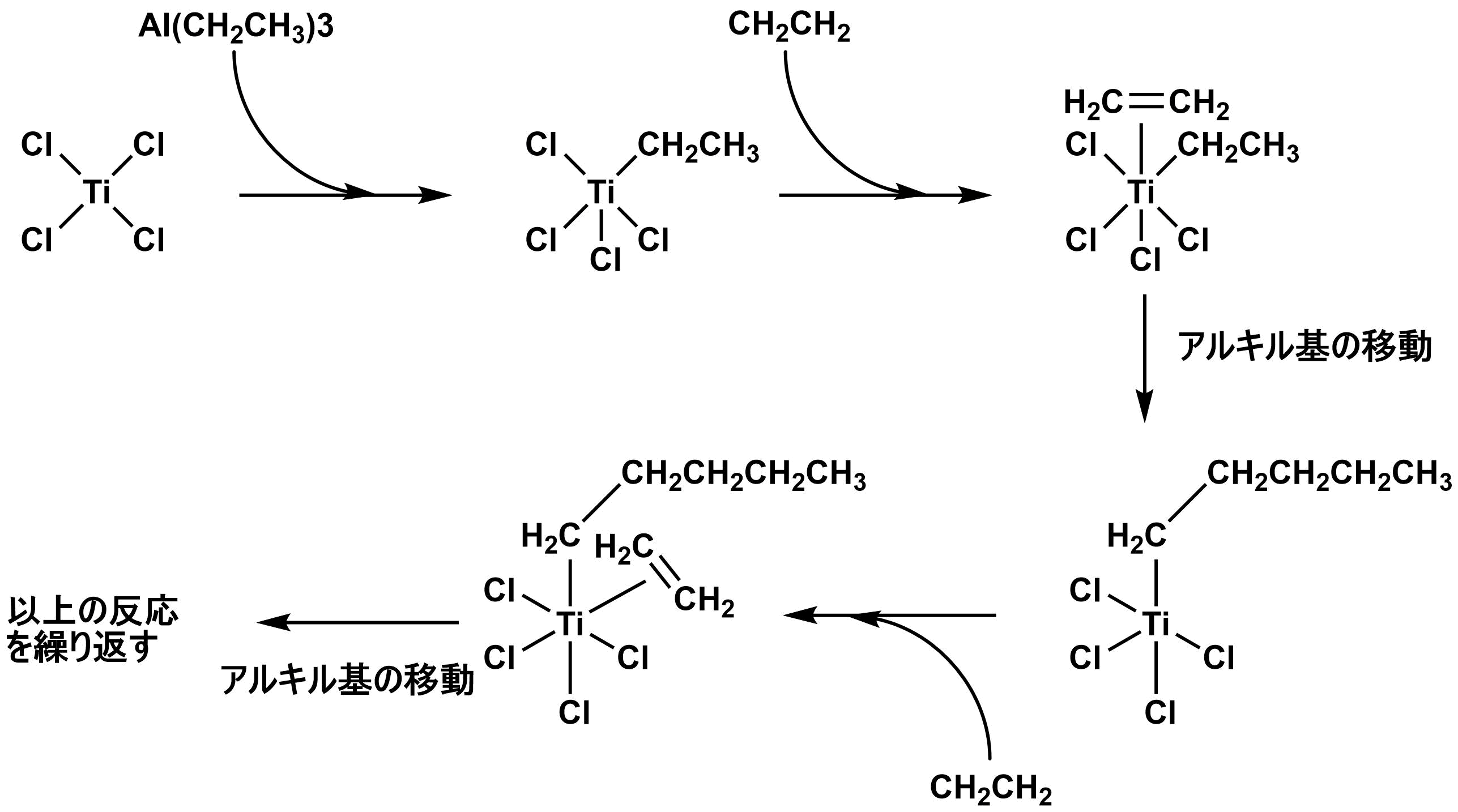 参考)レイナーキャナム無機化学 p399
参考)レイナーキャナム無機化学 p399




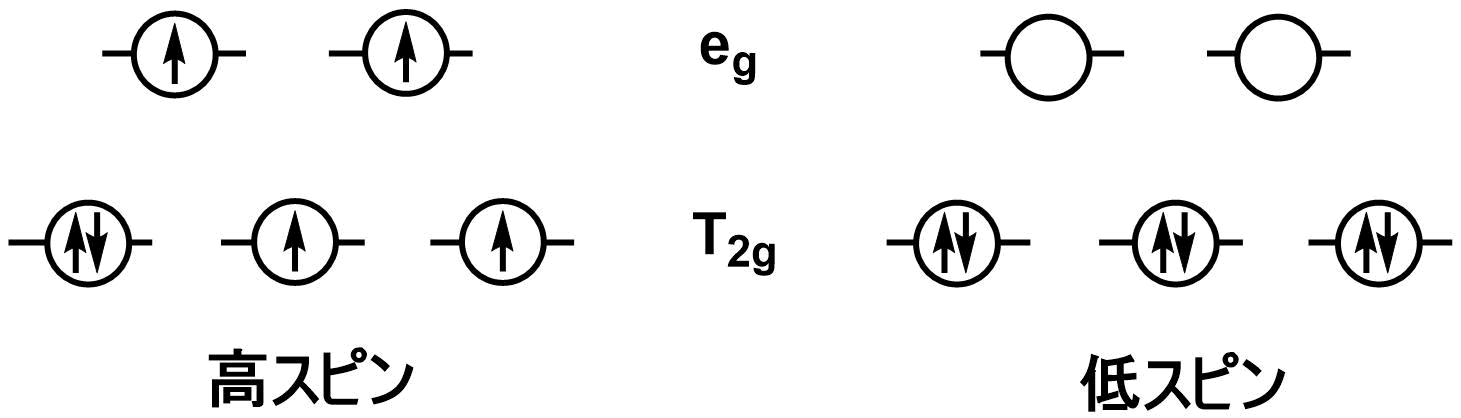
高スピンの磁気モーメント:$\sqrt{4(4+2)}=2\sqrt{6}=2×1.41×1.73=4.9[μ_B]$
低スピンの磁気モーメント:$\sqrt{0(0+2)}=0[μ_B]$

分光化学系列は、$\rm CN^->H_2O$なので、配位子場分裂エネルギーは$\rm CN^-$の方が大きい。よって、$\rm [Mn(H_2O)_6]^{2+}$のMnは高スピン、$\rm [Mn(CN)_6]^{4-}$は低スピン状態をとっていると思われる。この時、高スピンの方は$\rm d^5$で禁制遷移、低スピンは許容遷移になっているので$\rm [Mn(CN)_6^{4-}]$の方が吸光係数が大きくなる。
※スピン選択律について
入社してきた電磁場は、錯体中の電子スピンの相対的な配向を変えることはできない。たとえば、反平行スピンであった電子対を平行スピン対に変えること、つまり、一重項状態(S=0)を三重項状態(S=1)に遷移させることはできない。この制限は”スピン許容遷移はΔS=0”であるとまとめることができる。
$ΔS≠0$のスピン禁制遷移が観測される場合があるが、その強度はスピン許容遷移に比べて一般的にかなり小さい。原子番号が大きくなるにつれてスピン禁制遷移の強度が強くなるが、これは重原子の方が軽原子よりもスピンー軌道結合が強いからである。スピンー軌道結合によってスピン選択律が破られることをしばしば重原子効果という。
$d^5$の$\rm Mn^{2+}$イオン(高スピン)などはスピン許容遷移が無いため、ほとんど色を呈さない。
参考)シュライバー・アトキンス 無機化学 下 第6版 p637